7 stycznia 2026 roku w Journal of Neurology ukazał się artykuł opublikowany m.in. przez dr Magdalenę Mroczek, Prof. Magdalenę Chrościńską-Krawczyk, dr-a Stanleya Iyaduraia oraz dr-a Michała Bielaka – członków zespołu badawczego Fundacji PURA.
Zespół PURA poza innymi objawami charakteryzuje osłabienie mięśniowe, jednak mechanizm jego powstawania nie jest w pełni poznany. Zrozumienie tego, w jaki sposób dochodzi do osłabienia mięśni lub złącza nerwowo-mięśniowego na poziomie molekularnym może pozwolić na wdrożenie lepiej dobranego leczenia.
Pacjenci zostali zbadani przez neurologa dziecięcego- u wszystkich stwierdzono ciężkie zaburzenia rozwoju intelektualnego i osłabienie mięśniowe; u części z nich zaobserwowano problemy z oddychaniem (epizody bezdechu), nadmierną senność, oczopląs, problemy ze wzrokiem lub zez. U części pacjentów przeważały objawy mięśniowe (np. twarz miopatyczna, opadanie powiek, słabość mięśni karku) a część pacjentów miała cechy wrodzonego zespołu miastenicznego (CMS-Congenital Myasthenic Syndrome) tj. męczliwość wieczorem czy cechy CMS w badaniu elektrofizjologicznym.
Do badań molekularnych pobrano krew oraz wykorzystano niewielki fragment mięśnia od jednego pacjenta. Z preparatu mięśnia uda wyizolowano RNA, na którym wykonano badanie qPCR (Quantitative Polymerase Chain Reaction) w celu stwierdzenia, które geny ulegają zaburzonej transkrypcji. Przy pomocy spektrometrii mas określono również ilościowo które białka ulegają zaburzonej aktywności w próbce mięśnia i w pęcherzykach zewnątrzkomórkowych. Pęcherzyki zewnątrzkomórkowe to niewielkie struktury wydzielane przez komórki zawierające substancje sygnałowe – RNA, białka, sterole itp., które mogą służyć jako wskaźniki różnych chorób – nowotworów, chorób genetycznych i innych. Okazało się, że poziom białka TARSH używanego jako biomarker zespołów miastenicznych był znacząco obniżony, natomiast poziomy białek NOTCH2 i PON1 były podwyższone.
Wycinki mięśniowe zostały zbadane przy użyciu mikroskopu elektronowego. Badanie to wykazało niewielkie zmiany w m.in. architekturze złącza nerwowo-mięśniowego. Wyniki badań mikroskopii elektronowej nie wykazały żadnych specyficznych zmian.
Krew odwirowano, a oddzielone osocze zbadano przy pomocy testu ELISA na obecność nowo opisanego markera – białka odgrywającego kluczową rolę w działaniu złącza nerwowo-mięśniowego – trombospondyny 4 (TSP4). Pierwotnie marker ten został badany u pacjentów z rdzeniowym zanikiem mięśni, jednak może on znaleźć zastosowanie w diagnostyce osłabienia mięśniowego w zespole PURA. Co ciekawe, jest to biomarker, który ulegał normalizacji u pacjentów SMA leczonych lekiem Nusinersen, więc może on mieć zastosowanie nie tylko w diagnostyce chorób nerwowo-mięśniowych, ale też w monitorowaniu stanu klinicznego pacjenta poddanego leczeniu. U pacjentów z zespołem PURA stężenie markera TSP4 było 2,3 razy wyższe niż u pacjentów z grupy kontrolnej. Jednocześnie autorzy podkreślają ograniczenia pracy, w tym niewielką liczebność grupy badanej oraz analizę biopsji mięśnia pochodzącą od jednego pacjenta, co wymaga dalszych badań na większych grupach pacjentów.
Podsumowując, coraz więcej danych klinicznych, eksperymentalnych i terapeutycznych przemawia za możliwą rolą białka PURA w patologii złącza nerwowo-mięśniowego, jednak dokładna lokalizacja białka PURA pozostaje niewyjaśniona. Badanie wskazało potencjalne markery i zmiany molekularne, które mogą być podstawą do dalszych badań i do zaprojektowania terapii w zespole PURA.
Autor Hubert Kubiszewski, red. Dr med. Magdalena Mroczek
Na podstawie: Mroczek M, Preusse C, Hentschel A, Chrościńska-Krawczyk M, Bielak M, Sobolewska A, Della Marina A, Hila A, Iyadurai S, Kraft F, Chetty VK, Muhmann D, Ruck T, Goebel HH, Schara-Schmidt U, Dobelmann V, Thakur BK, Stenzel W, Roos A. Exploring molecular signatures in PURA syndrome using muscle proteomics and serum biomarkers. J Neurol. 2026 Jan 23;273(2):94. doi: 10.1007/s00415-026-13621-7. PMID: 41575592; PMCID: PMC12830457.
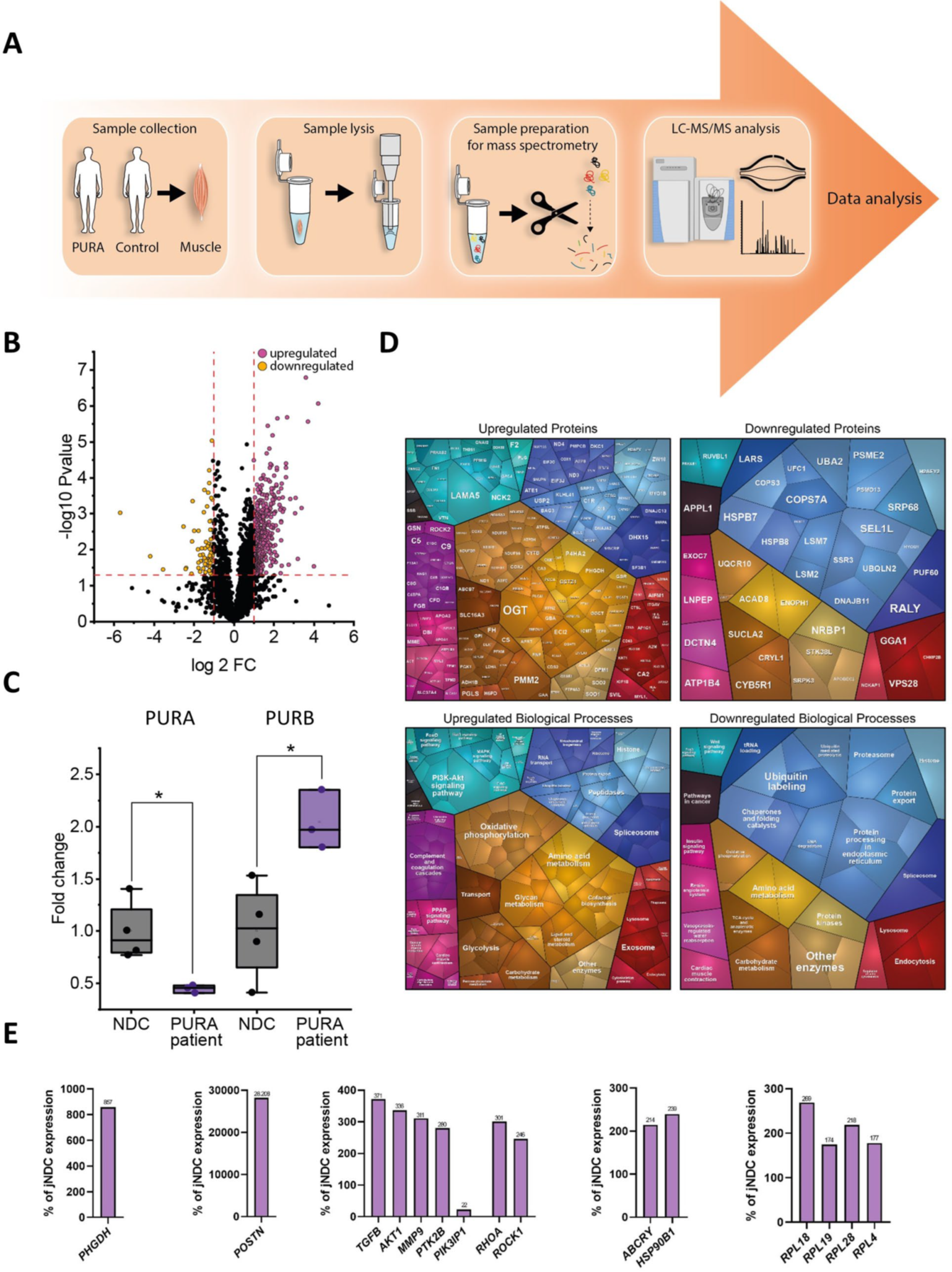
A. Schemat eksperymentu i kolejno wykonywanych badań
B. Wykres przedstawiający nadmiernie aktywne (na fioletowo) lub za mało aktywne białka (na żółto)
C. Wykres przedstawiający zmniejszoną aktywność białka PURA i zwiększoną aktywność białka PURB w próbce mięśnia w porównaniu do zdrowej kontroli
D. Analiza in silico białek o zaburzonej aktywności. Pierwszy rząd przedstawia konkretne białka o zaburzonej aktywności, natomiast drugi- zaburzone procesy biologiczne zależne od powyższych białek dla białek o zwiększonej (lewa kolumna) lub zmniejszonej aktywności (prawa kolumna)
E. Analiza transkryptów genów szlaków periostyny oraz modulatorów ekspresji periostyny w porównaniu ze zdrową grupą kontrolną wykazuje znacznie zwiększoną ekspresję. Dodatkowo na podstawie wzrostu ilości białek rybosomalnych w mięśniu z mutacją PURA, poziom transkryptów białek rybosomalnych również wykazał wzrost dla wszystkich odpowiadających im transkryptów.
Źródło: Mroczek, M., Preusse, C., Hentschel, A., Chrościńska-Krawczyk, M., Bielak, M., Sobolewska, A., Della Marina, A., Hila, A., Iyadurai, S., Kraft, F., Chetty, V. K., Muhmann, D., Ruck, T., Goebel, H.-H., Schara-Schmidt, U., Dobelmann, V., Thakur, B. K., Stenzel, W., & Roos, A. (2026). Exploring molecular signatures in PURA syndrome using muscle proteomics and serum biomarkers. Journal of Neurology, 273(2). https://doi.org/10.1007/s00415-026-13621-7
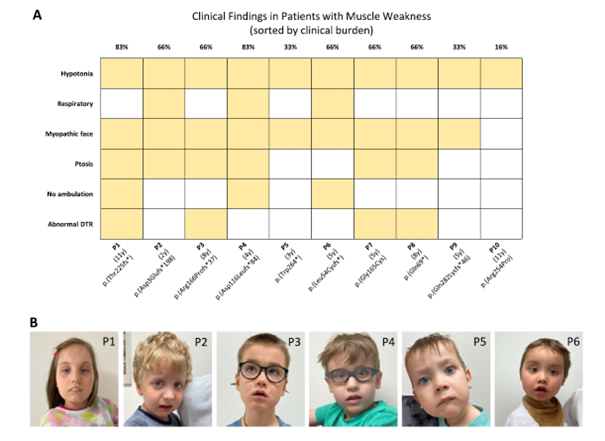
A. Tabela przedstawia obecność (na żółto) lub brak (na biało) obecność sześciu objawów u dziesięciu pacjentów z zespołem PURA (P1-P10). Cechy te zostały wybrane w oparciu o ich powiązanie kliniczne z zespołem PURA lub innymi chorobami dotykającymi złącza nerwowo-mięśniowego. Pierwszy wiersz to zakodowany numer pacjenta, drugi to wiek pacjenta w czasie badania, a trzeci – wariant genetyczny (które aminokwasy w białku uległy zmianie wskutek mutacji). Objawy zostały wyróżnione na pionowej osi: osłabienie mięśniowe, zaburzenia oddychania, twarz miopatyczna, ptoza, czy pacjent jest chodzący i nieprawidłowe głębokie odruchy ścięgniste. Należy zaznaczyć, że w zaburzenia oddychania zostały włączone bezdechy senne bez przewlekłej niewydolności oddechowej lub uzależnienia od zewnętrznej wentylacji, a w nieprawidłowe odruchy ścięgniste oznaczają (wygórowane lub osłabione)
B. Zdjęcia sześciu pacjentów (P1-P6) wykazujących objawy uszkodzenia złącza nerwowo-mięśniowego, takich jak ptoza (P1 i P6), osłabienie mimiki twarzy i otwarte usta (P1-P4 i P6) i zez (P1 i P6).
Źródło: Mroczek, M., Preusse, C., Hentschel, A., Chrościńska-Krawczyk, M., Bielak, M., Sobolewska, A., Della Marina, A., Hila, A., Iyadurai, S., Kraft, F., Chetty, V. K., Muhmann, D., Ruck, T., Goebel, H.-H., Schara-Schmidt, U., Dobelmann, V., Thakur, B. K., Stenzel, W., & Roos, A. (2026). Exploring molecular signatures in PURA syndrome using muscle proteomics and serum biomarkers. Journal of Neurology, 273(2). https://doi.org/10.1007/s00415-026-13621-7

